真核生物的
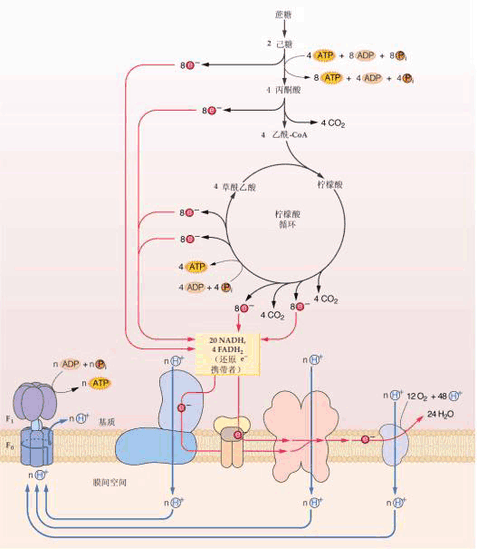
许多生化代谢过程,如糖酵解、三羧酸循环和β氧化,都会产生还原型辅酶NADH。此辅酶含有高电极电势的电子;也就是说,它们将在氧化时释放出大量的能量。然而,细胞不会一次性释放完全部的能量,因为在这种情况下,反应将无法控制。相反,电子从NADH释放出来,并通过一系列的酶传递给氧气,其中每步只释放少量的能量。由复合体I到IV组成的这组酶称为电子传递链,存在于线粒体内膜中。琥珀酸也被电子传递链氧化,但起点不同。 真核生物中,电子传递系统中的酶用从氧化NADH释放的能量,泵送质子穿过线粒体内膜。这会使质子在膜间隙中积聚,产生跨膜电化学梯度。然后,ATP合酶使用存储在其中的势能以产生ATP。其中,真核细胞线粒体中的氧化磷酸化是这一过程研究最为透彻的样例。线粒体存在于几乎所有的真核生物中,但部分原生生物例外,如阴道毛滴虫中称为氢化酶体的残留线粒体会将质子还原为氢。 呼吸酶 | 氧化还原对 | 中点电位(伏) |
NADH脱氢酶 | NAD/NADH | −0.32 |
琥珀酸脱氢酶 | | −0.20 |
细胞色素bc复合体 | 辅酶Q10/ 辅酶Q10 | +0.06 |
细胞色素bc复合体 | 细胞色素b/ 细胞色素b | +0.12 |
展开表格
NADH-Q还原酶,又称“NADH脱氢酶”或“复合体I”,是电子传递链中的第一个蛋白。它是一个巨大的酶,在哺乳动物中该复合体由46亚基组成,有1000千道尔顿(kDa)。目前只了解一种细菌的复合体详细结构;大多数生物的复合体酷似有一个大“球”的靴子,从膜中穿到线粒体。编码单个蛋白质的基因同时包含在细胞核和线粒体基因组中,许多线粒体酶都是这种情况。 此酶催化的反应为NADH被辅酶Q10,即线粒体膜上的一种脂溶性醌类“泛醌”(在下面公式中写作Q)所氧化,同时转移两个电子: 这个反应乃至于整个电子链,是从NADH分子与复合体I结合及放出两个电子而开始。电子通过附着在其上的黄素单核苷酸(FMN)辅基进入复合体I。电子的加入使FMN转换为它的还原形式,FMNH。电子随后通过一系列存在于复合体中的第二种辅基铁硫簇转移。复合体I中存在两种铁硫簇,[2Fe-2S]和[4Fe-4S]。 电子穿过复合体时,有4个质子从基质泵入膜间隙。尚不清楚其中的机制,但似乎与复合体I的构象改变有关,这可使该蛋白质在膜的N侧结合质子,并在P侧释放它们。最后,电子从铁硫簇链转移到膜中的泛醌分子上。泛醌的还原也有助于质子梯度的产生,因为基质中的两个质子被用于泛酚(QH)的还原。
琥珀酸-Q氧化还原酶,又称“复合体II”或“琥珀酸脱氢酶”,是电子传递链的第二个入口。它很特别,因为它是唯一一个既属于三羧酸循环、又属于电子传递链的酶。复合体II包含四个蛋白质亚基,一个附着的黄素腺嘌呤二核苷酸(FAD)辅因子,铁硫簇,和一个不参与将电子转移到辅酶Q、但被认为在降低氧化物活性上起重要作用的血红素基团。它将琥珀酸氧化为延胡索酸,将泛醌还原。该反应释放的能量比氧化NADH少,因此复合体II不运输质子穿过膜,不会影响质子梯度。 一些真核生物,如寄生虫猪蛔虫,有类似复合体II的延胡索酸还原酶(甲基萘醌:延胡索酸氧化还原酶,又称QFR),但功能相反,其氧化泛醌而还原延胡索酸。这使蠕虫可以在大肠的厌氧环境中生活,将延胡索酸作为电子受体进行厌氧氧化磷酸化。复合体II的另一种非常规功能在引起疟疾的寄生虫“恶性疟原虫”中得到体现。在这里作为氧化酶,复合体II的逆作用对泛酚的再生很重要,寄生虫将其用于一个不寻常的生物合成嘧啶的方式。 电子传递黄素蛋白-Q氧化还原酶
电子传递黄素蛋白-泛醌氧化还原酶(ETF-Q氧化还原酶),又称“电子传递-黄素蛋白脱氢酶”,是电子传递链的第三个入口。它是接收线粒体基质中电子传递黄素蛋白的电子,并用这些电子还原泛醌的酶。这种酶包含一个黄素和一个[4Fe-4S]簇,但不像其它的呼吸链复合体,它只附着在膜的表面,不跨越脂质双分子层。 哺乳动物中,该代谢途径在脂肪酸的β氧化和氨基酸及胆碱的分解代谢作用中很重要,因为它接受来自多个乙酰辅酶A脱氢酶的电子。在植物中,ETF-Q氧化还原酶也对使植物可以在长时间的黑暗中生存下来的代谢反应重要。 Q-细胞色素c氧化还原酶(复合体III)
Q-细胞色素c氧化还原酶又称“细胞色素c还原酶”、“细胞色素bc复合体”,或简称“复合体III”。在哺乳动物中,这种酶是一个二聚体,每个亚基包含11个蛋白质亚基,1个[2Fe-2S]铁硫簇和3个细胞色素:1个细胞色素c和2个细胞色素b。细胞色素是一种传输电子的蛋白,包含至少一个血红素基团。当电子通过蛋白传递时,复合体III中血红素基团内的铁原子在还原型二价铁(+2)和氧化型三价铁(+3)之间切换。 复合体III催化的反应是一分子泛酚的氧化和两分子细胞色素c的还原,血红素蛋白部分与线粒体相关。不同于辅酶Q携带两个电子,细胞色素c只携带一个电子。 作为反应中唯一可将电子从QH供体转移到细胞色素c受体的物质,复合体Ⅲ的反应机理较其他呼吸复合物认识更为详尽,其包含两个步骤,称作Q循环。首先在第一步中,酶与三个QH底物结合,然后将其氧化,并将所产生的一个电子传递到第二个底物细胞色素C。QH所释放的两个质子被传递到膜间隙。第三个底物Q接受来自QH的第二个电子,而还原为泛半醌自由基Q。先前的两个底物被释放,但这个泛半醌中间体仍然被酶所结合。第二步中,第二个QH分子与酶结合,再一次将它的第一个电子传递给细胞色素c受体。结合的泛半醌得到第二个电子,并获得线粒体基质中的两个质子,而还原为QH。这个QH随后被酶释放。 当辅酶Q在膜的内侧还原为泛酚,而在另一面氧化为泛醌时,质子的跨膜净转移随之发生,从而增加了质子梯度。通过相当复杂的两步机制完成反应是重要的,因为它增加了质子转移的效率。如果替换Q循环,直接用一个QH分子来还原两个细胞色素c分子,则每还原一个细胞色素c只能传送一个质子,效率将会减半。
细胞色素c氧化酶(复合体IV)
细胞色素c氧化酶,又称“复合体IV”,是在电子传递链的最后一个蛋白质复合体。哺乳动物的酶有极其复杂的结构,包含13个亚基,2个血红素基团,以及多种金属离子辅因子——总计3个铜原子,1个镁原子和1个锌原子。
这种酶承载了电子传递链的最终反应,在跨膜泵送质子时将电子转移到氧上。这一步,氧作为最终电子受体,也称“末端电子受体”,被还原为水。直接泵送的质子和在氧的还原中消耗的基质中质子都能影响质子梯度。所催化的反应为细胞色素c的氧化及氧的还原:
替代的还原酶和氧化酶
许多真核生物的电子传递链中的酶与上述研究较多的哺乳动物有所不同。例如,植物有替代的NADH氧化酶,可以不在线粒体基质而在细胞质中氧化NADH,并将这些电子传递到泛醌池。这些酶不传送子,可在不改变跨膜电化学梯度时还原泛醌。
分岔电子传递链的另一个例子是“替代氧化酶”,存在于植物、一些真菌及原生生物中,一些动物也可能包含其中。这种酶可直接将泛酚中的电子转移到氧。
通过这些替代NADH和泛醌氧化酶的电子传递途径比完整路径的ATP产量低。这些捷径的优点尚不明确。然而,替代氧化酶产生于应激反应,如受寒、活性氧、病原体感染,及其他抑制完整电子传递链的因素。因此,替代途径可能可以通过减少氧化应激,从而提高生物对伤害的抵抗力。
复合体组织
最初的呼吸链复合体组织模型认为它们互相独立,在线粒体膜中自由扩散。然而,最近的数据表明,复合体可能形成称为超复合体或“呼吸体”的高级结构。在此模型中,各个复合体存在于有相互作用酶的有序集合中。这些关联可能使各种酶复合体之间建立了底物通道,增加电子转移的速率和效率。在哺乳动物的这些超复合体中,某些部件的数量可能较其它的要多,部分数据表明复合体I/II/III/IV和ATP合酶的比大致为1:1:3:7:4。然而,对超复合体假说的争论仍未完全结束,因为部分数据似乎无法支持此模型。