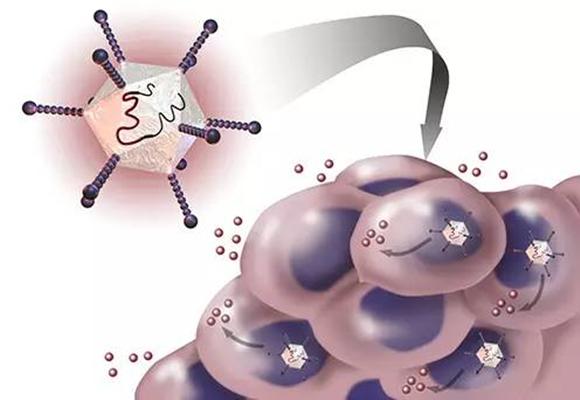
腺病毒是一种大分子(36kb)双链无包膜DNA病毒。它通过受体介导的内吞作用进入细胞内,然后腺病毒基因组转移至细胞核内,保持在染色体外,不整合进入宿主细胞基因组中。
腺病毒载体相关的文章
灵笼艺画开天与bilibili联合出品的动画本词条是多义词,共3个义项《灵笼》是由艺画开天、bilibili联合出品,艺画开天制作,董相博执导,李元韬、陶典、黄莺配音的原创网络动画作品。该动画讲述了在未来,地球经历了一场毁灭性的浩劫,幸存的人类不得不避难于一座悬浮于空中的灯塔上,继而面对地面上的邪恶
牤牛为哺乳动物,草食性,部分种类为家畜(包含家牛、黄牛、水牛和牦牛)。体型粗壮,部分公牛头部长有一对角。公牛俗称牤牛,也称牯牛,小牛俗称牛犊。牛还具多种用途:肉和乳可供食用,牛皮可做工业原料及衣料,牛角可做药材及工艺品等;牛还可为农业生产等提供役力。
十字军(The Crusaders),由天主教士兵组成的军队,曾参加十字军东征,士兵都佩有十字标志,因此称为十字军。十字军东征的目的是保护朝圣者和反对吉哈德扩张,以及从伊斯兰诸国手中拯救半奴隶与奴隶并缓解突厥人对君士坦丁堡的压力。在十字军的帮助下,拜占庭帝国成功收复尼西亚、吕底亚、密细亚、弗里吉亚北
高僧高僧:宋代文物陶模高僧宋代(960年—1279年)开封基本信息出土地点东京所属年代宋代基本信息【藏品名称】:高僧【藏品现状】:开封大学大观博物馆收藏藏品介绍高僧宋代(960年—1279年)开封HierarchSongDynasty(960–1279A.D.
偏瘫急性脑血管病的常见症状偏瘫(hemiplegia)又叫半身不遂,是指同一侧上下肢、面肌和舌肌下部的运动障碍,是急性脑血管病的常见症状。轻度偏瘫病人虽然尚能活动,但走起路来,往往上肢屈曲,下肢伸直,瘫痪的下肢走一步划半个圈,这种特殊的走路姿势,叫做偏瘫步态。严重者常卧床不起,丧失生活能力。按照偏瘫的程度,可分为轻瘫、不完全性瘫痪和全瘫。轻瘫:表现为肌力减弱,肌力在4~5级,一般不影响日常生活,不

尚可名片
这家伙太懒了,什么都没写!