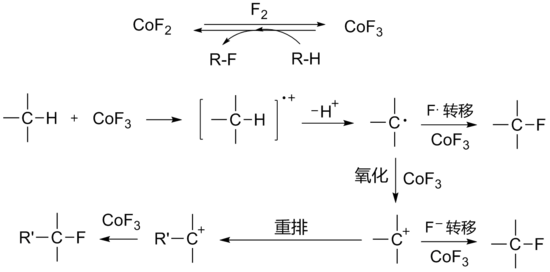
三氟化钴(化学式:CoF3),IUPAC名称氟化钴(III),室温下为不稳定的浅棕色易潮解固体,溶于水放出氧气,是很常用的氟化剂,用于有机氟化合物(尤其是全氟化合物)的制取,还原产物是二氟化钴。
精选百科
本文由作者推荐
三氟化钴相关的文章
蜜蜂属是一种社会性全变态昆虫,在分类学上属于蜜蜂科蜜蜂属昆虫。原始的蜜蜂属出现于渐新世,距今已有3000~4000万年。蜜蜂营群体生活,生活在蜂巢里。每一个蜂群由蜂王、雄蜂、工蜂组成。它们形态特征各不相同,蜂王的身体最大,腹部末端有螫针,是和别的蜂王相斗的工具,它的生殖系统发达,可以活4~5年。雄蜂
布拉格是捷克共和国的首都和最大的城市,位于该国的中波希米亚州、伏尔塔瓦河流域。该市地处欧洲大陆的中心,在交通上一向拥有重要地位,与周边国家的联系也相当密切。布拉格的面积为496平方公里,截至2022年1月,人口约为127.5万。布拉格是一座欧洲历史名城,城堡始建于公元9世纪。1345—1378年,在
白宫本词条是多义词,共2个义项美国总统的官邸和办公室白宫(英语:The White House)也称为白屋,是美国总统的官邸和办公室。1901年被西奥多·罗斯福总统正式命名为“白宫”。白宫由美国国家公园管理局拥有,是“总统公园”的一部分。白宫是一幢白色的新古典风格砂岩建筑物,位于华盛顿哥伦比亚特区西北宾夕法尼亚大道1600号。白宫共占地7.3万多平方米,由主楼和东、西两翼三部分组成。

尚可名片
这家伙太懒了,什么都没写!
作者