简介
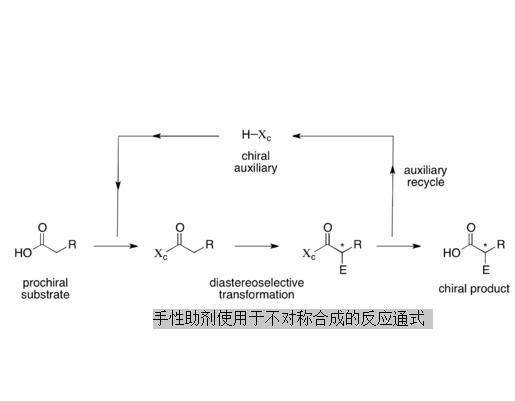
手性助剂使用于不对称合成的反应通式
手性助剂是不对称合成的新技术,均是对映体化合物,这些化合物通过共价键暂时与底物相连接。在该底物以后所进行的反应过程中,这些手性助剂诱导出所希望的手性或使生成的对映体之一过量,最后再将这些助剂裂掉回收。一个例子是(S,S)A-74704的合成,该化合物是HIV蛋白酶抑制剂,是治疗艾滋病的一种候选药物。另一个例子:手性助剂(2,5-二甲基吡咯烷)先与环已酮反应,以诱导立体选择反应,然后脱去,对映体过量达80%。大部分的生物分子和标靶药物存在着两种可能的镜像异构物(又称对映异构)中的其中一种;因此,天然产物和药物试剂的化学合成通常被设计成获得目标在单一镜像化合物(enantiomerically pure)的形式。化学家会使用很多方法去合成所期望的立体异构物,而加入手性助剂即为方法之一。
非对称合成
为了控制化合物立体中心的绝对构造,手性助剂会在合成途径中被结合。在众多使用手性助剂的合成中David A.Evans cytovaricin的合成被认为是经典。他利用一个不对称烷基化反应和四个不对称羟醛缩合反应而成的噁唑烷酮手性辅助剂,产生出有9个立体中心的绝对立体化学结构。
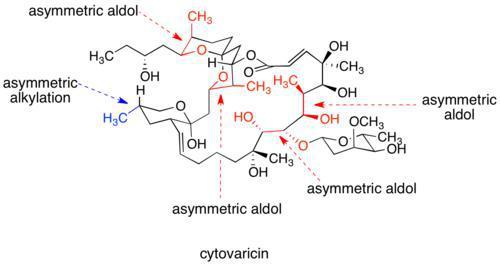
Cytovaricin
如图是Cytovaricin,于1990年被D.A.Evans所合成出来的产物。蓝色及红色的键结表示用手性助剂镶嵌出的立体结构中心。一个典型反应在辅助引导下的立体选择性转化需要三个步骤:首先,由辅助剂共价结合在基板上;接着,所产生的化合物会进行一或多种非镜像选择性(diastereoselective)的转换;而最后,辅助剂在不会引起所需产物外消旋化(racemization)的情况下被移除。使用化学剂量辅助剂花费的能量加上合成步骤中结合和除去所需的能量使得此途径似乎较没效率。然而,对许多转化物来说,可以产生立体选择性的方法必须依赖手性助剂。此外,使用手性助剂的转换趋于多用途且好研究,从而使得单一镜像异构物的获得变得最为省时。
更进一步说明,在辅助剂引导反应下的产物为非镜像异构物(或称非对映异构),能使他被一些方法如管柱层析法(column chromatography)或是结晶做简单分离。
几种常见的手性助剂
8-苯基薄荷醇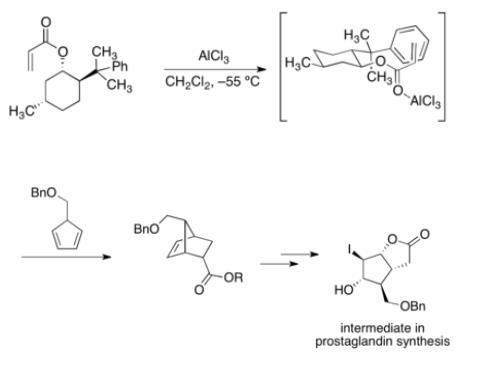
手性助剂(-)-8-苯基薄荷醇来合成前列腺素
在先前手性助剂使用于不对称合成的范例中常用的是8-苯基薄荷醇丙烯酸酯和5-苄氧甲基环戊二烯(5-benzyloxymethylcyclopentadiene)之间的不对称双烯加成反应(狄耳士–阿德尔反应)。而环化反应后的产物碘代内酯(iodolactone)如图所示,为典型Corey反应中,前列腺素合成的中间产物。因为丙烯酸酯的背面被辅助剂阻挡,所以环化反应只能发生在烯烃的前方。噁唑烷酮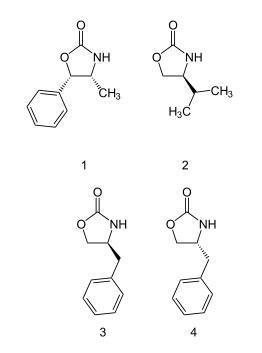
几种常见的噁唑烷酮手性辅助剂
噁唑烷酮(2-Oxazolidone)辅助剂,由大卫·A·伊凡斯普及于世,已经被应用到许多立体选择性转换上,包括羟醛缩合反应、烷基化反应,和狄尔斯-阿尔德反应(又称双烯加成反应)。噁唑烷酮取代4和5位置。透过空间位阻(立体阻碍),因此取代基引导了各种基团取代的方向。而辅助剂便随后被除去,例如:透过水解的方式。噁唑烷酮可以从氨基酸或从容易取得的氨基醇(Alkanolamine)中制备出。大量的噁唑烷酮是有市售的,包括如图四种。
噁唑烷酮酰亚胺加上强碱,像是二异丙基氨基锂能选择性提供(Z)-烯醇的强碱,噁唑烷酮酰亚胺的α碳去质子化,最终它可以进行立体选择性烷基化。
噁唑烷酮辅助剂在立体选择性的羟醛缩合反应是最为广泛使用的。使用三氟甲磺酸二丁硼作为路易士酸和二异丙基乙胺作为碱所形成的软烯醇化反应,会产生出(Z)-烯醇化物。而此化合物可用醛当作基板形成非镜像选择性的羟醛缩合反应。这种转化是非常有能量的,因为它形成了两个连续的立体结构中心。
硫酸伪麻黄碱(R,R)-和(S,S)-硫酸伪麻黄碱皆可作为手性助剂。硫酸伪麻黄碱与羧酸、酸酐和酰氯反应形成硫酸伪麻黄酰胺(pseudoephedrine amide)。
羰基的α-质子很容易被非亲核碱移除,而近一步形成烯醇化物(enolate)。加成化合物的构造是被甲基所导向的,例如卤代烷。因此,任何加成产物与甲基成反相位,而与羟基成同相位。硫酸伪麻黄碱手性助剂的后续移除,是借由适当的亲核试剂切除酰胺键而完成。
硫酸伪麻黄碱的两种镜像异构物皆可市售。外消旋硫酸伪麻黄碱是市售的苏达菲(Sudafed)以及其他品牌的鼻腔解充血剂。因为硫酸伪麻黄碱可以转化为非法物质甲基苯丙胺,所以不管是学术用途或工业研究上的购买,都是受到监管的。
硫酸伪麻黄酰胺的非镜像选择性被认为是结构所造成的,因为烯醇锂的其中一个面向,会被醇化锂和与锂阳离子有关的溶剂分子阻挡住。根据此说法指出,在烷基化步骤的非镜像选择性高度依赖于氯化锂的存在量与所使用的溶剂,四氢呋喃(THF)。一般来说,4到6当量的氯化锂就足以让烯醇化物在THF溶液中的反应莫耳浓度达到饱和。
工业上的手性助剂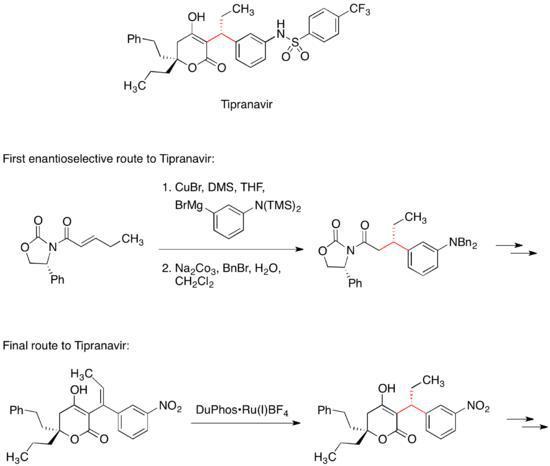
HIV蛋白酶抑制剂的合成
手性助剂通常是可靠且多功能的,使得大量的单一镜像异构物可在省时的方式下合成。因此,手性助剂经常会在药物开发的初期阶段被使用。(1)HIV蛋白酶抑制剂(Tipranavir):
HIV蛋白酶抑制剂(Tipranavir)被销售用于艾滋病的治疗。Tipranavir在药物化学用途中的第一镜像选择性,包括有机酮试剂的共轭加成手性麦可受体。Michael受体中的噁唑烷酮控制着此两立体中心中其中一个的立体性。(2)阿托伐他汀(Atorvastatin):
阿托伐他汀的钙盐在市场上的销售名为立普妥(Lipitor)是一种降低血中胆固醇的药物。Atorvastatin在药物化学用途中的第一镜像选择性依赖著非镜像选择性的醇醛缩合反应,而反应中使用手性酯来建立醇的两个立体中心的其中一个。Atorvastatin在商业用途上因容易获得的异抗坏血酸而被发扬光大。
