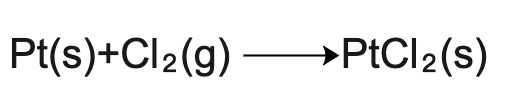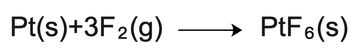铂 铂
铂(英文名,platinum),俗称白金,元素符号Pt,原子序数78,原子量195.09,属周期系第Ⅷ族元素,铂是一种密度高、延展性高、反应性低的灰白色贵金属,属于过渡金属。铂有六种稳定的同位素:铂-190、铂-192、铂-194、铂-195、铂-196、铂-198。铂的化学性质不活泼,在空气中不会氧化,但可被卤素、 氰化物 、硫和碱腐蚀。铂不溶于 盐酸 ,硝酸,硫酸和碱溶液,但可以溶于 王水 ,形成 氯铂酸 (H₂PtCl₆)。铂的应用包括:珠宝首饰、实验室用的电线和容器、电触头、电阻温度计、玻璃系统中的密封电极、抗腐蚀仪器、牙科器材、石油裂解和 燃料电池 的催化剂、抗腐蚀仪器。含铂的化合物,比如顺铂(PtCl₂( NH3 )₂),可以用于治疗某些类型的癌症,如白血病或 睾丸癌 等。
发现历史 铂是一种极其罕见的金属,在地壳中的浓度仅为3.7×10⁻⁶%(按重量计算)。它最初是在前 哥伦布 时代,被南美土著用来制作鼻环、耳环和面具等工艺品 。1557年意大利人类学家朱利斯·凯撒·斯卡利杰(Julius Caesar Scaliger)写到在墨西哥和巴拿马发现了一种从未见过的贵金属,但这种金属被认为是金中的杂质 。 西班牙人 安东尼奥·德·乌略亚(Antonio de Ulloa)被认为是第一位描述铂金属科学家。1735年,他在穿越 哥伦比亚 和 秘鲁 的途中,注意到土著 印第安人 会开采一种白色的像银一样的金属,他们把样品带回了西班牙。他们将这种新金属取名为platinum,源自西班牙文platina,意思是银。他把铂描述为“不可分离且不可煅烧的金属”。 另外一些人认为英国 牙买加 发现了来自哥伦比亚的铂样本,他将这些样本送到威廉-布朗里格处进行进一步的分析研究。1750年,在研究了伍德送的样本后,布朗里格向英国皇家学会详细的介绍了这种金属,表示之前在任何已知矿物中都没有提及这种金属的存在。布朗里格还发现铂具有极高的熔点。之后,包括 永斯·雅各布·贝采利乌斯 (Jöns Jakob Berzelius),安德烈亚斯·西吉斯蒙德·马格拉夫(Andreas Sigismund Marggraf),托贝恩·奥洛夫·贝格曼(Torbern Olof Bergman),威廉·李维斯(William Lewis)和皮埃尔·约瑟夫·马盖(Pierre Joseph Macquer)等在内的欧洲科学家都开始对铂进行研究。1752年,亨利克·特奥菲卢斯·谢佛尔(Henrik Teofilus Scheffer)发表了更详细的报道来描述铂,他将这种金属称为“白金”,并且表述了如何利用砷来熔融铂矿物。1772年,卡尔·冯·西金根(Carl von Sickingen)制造了可塑性的铂。
分布情况
铂矿的发现历史 目前世界开发矿山生产铂的有南非、俄罗斯、加拿大、津巴布韦、美国和中国等6个国家 。历史上,与阿拉斯加— 乌拉尔 型 块状矿石 曾是世界铂金的唯一开采来源。随后1823年,在俄罗斯乌拉尔发现了丰富的铂金矿床。接着1885年,在加拿大不列颠哥伦比亚省的 泰晤士河 (Thames River)开采了块状铂金。来自哥伦比亚、乌拉尔和不列颠哥伦比亚的铂铁矿块通常与 铬铁矿 和橄榄石密切相关。如今,块状铂金(主要为 铂铁合金 )的产量约占世界产量的1-2%。 铂族金属矿床可以分为六类:镁铁质—超镁铁质层状岩体型、镁铁质—超镁铁质Cu-Ni硫化物矿床伴生型、Urals杂岩体型、 蛇绿岩 型、热液型和外生型。另外根据铂族元素的容矿岩石类型、 元素共生组合 、矿床地质特征和产出的地质环境等要素,也有学者将铂族元素矿床划分为岩浆型、热液型、火山岩块状硫化物型(VMS)和外生型四大类型。 铂金属产地主要集中 美国地质调查局 统计,近五年(2016-2021)世界铂金属产量如下表所示 : 铂/t
2016
2017
2018
2019
2020
2021
美国
3.9
3.9
4.1
3.6
4
4.2
加拿大
9
12
9.5
7.4
7.8
6
俄罗斯
23
21
21
22
21
19
南非
120
140
110
130
120
130
津巴布韦
13
15
14
15
14
15
其他国家
3.4
4
6.1
4.3
3.8
4.3
总产量
172
200
160
180
170
180
截止2021年,世界 铂族金属 储量为70000t,储量排名前五的国家分别为南非(63000t)、俄罗斯(4500t)、津巴布韦(1200t)、美国(900t)、加拿大(310t)。
理化性质
物理性质 密度属性
固体密度
21.45 g/cm³
弹性特性
杨氏模量
168 GPa
摩尔体积
9.09 cm³
体积模量
230 GPa
硬度
莫式硬度
5.5
剪切模量
61 GPa
维式硬度
549MN m²
泊松比
0.38
布什硬度
392MN m ⁻²
电气特性
电阻率
1.6 × 10⁻⁸Ω m
热和传导
导热系数
72W m⁻¹K⁻¹
光学特性
反射率
73%
线性热膨胀系数
8.8×10⁻⁶ K⁻¹
声学特性
声速
2680m/s
铂的同位素主要有6种:
同位素
大小/Da
丰度(%)
核自旋
磁矩(μ/μN)
¹⁹ºPt
189.959917
0.014
0
0.6095
¹⁹²Pt
191.961019
0.782
0
¹⁹⁴Pt
193.962655
32.967
0
¹⁹⁵Pt
194.964766
33.832
1/2
¹⁹⁶Pt
195.964926
25.242
0
¹⁹⁸Pt
197.967869
7.163
0
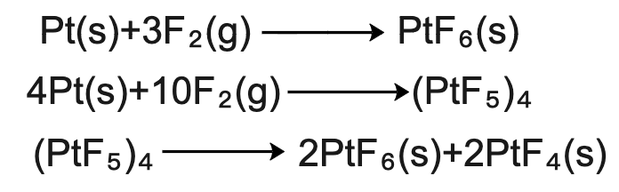
化学性质 铂的化学性质稳定,在空气和潮湿环境中不被氧化,常温下不易被酸、碱、盐和有机物等腐蚀,能耐 硫蒸气 、汞、熔融的硫酸盐、 氯化物 、碳酸盐和熔化玻璃的侵蚀。铂溶于热的王水和熔融碱。高温下铂能与硫、磷、卤素等发生作用。铂易形成配位化合物。在加热时铂仍保持原有光泽。在450℃以下有明显可见的 二氧化铂 氧化薄膜生成,450℃以上二氧化铂分解挥发而使铂缓慢失重。高温下,铂与硅会熔成合金,从而降低铂的质量。 铂和 氟气 (F₂)发生反应,会产生挥发性的氟化铂(PtF₆)或 四聚体 结构的氟化铂(PtF₅)。后者与氟化铱(IrF₅),氟化铑(RhF₅),氟化锇(OsF₅)和氟化钌(RuF₅)具有相同的结构类型 。 金属铂和氯气(Cl₂)根据反应条件不同,会形成两种不同形式的 氯化铂 (PtCl₂) 。
制备方法
铂族金属 铂族金属的冶金过程可分为富集和精炼两段。常用的富集技术包括高温焚烧富集技术、高温熔炼富集技术和湿法富集技术,根据物料的种类与形态,采用不同的方法富集铂族金属。
(1)高温焚烧富集技术:各种炭 载体催化剂 、树脂催化剂、含铂族金属的有机废料主要采用高温焚烧炉焚烧富集 。高温下,有机物被氧化分解成无毒的CO₂和水蒸汽,铂族金属富集在焚烧渣中。 (2)高温熔炼富集技术采用等离子熔炼炉、电弧熔炼炉以铁、铜、高冰镍为捕集金属从汽车尾气净化废催化剂、化工类氧化铝载体催化剂、玻纤 浇铸料 、硝酸工厂的炉灰、铂族金属湿法冶炼残渣和精炼残渣中回收铂族金属。 (3)含铂族金属的湿法富集技术包括:溶解技术、化学剥离技术、置换技术、吸附技术等,根据物料类别,采用不同的湿法富集技术。以 γ - Al₂O₃ 为载体含铂族金属催化剂主要有Pt/Al₂O₃、Pt-Re/Al₂O₃、Pt-Sn/Al₂O₃、Pd/Al₂O₃,将载体溶解后,铂族金属不被溶解而富集在溶解渣中,形成高含量的铂族金属精矿。 铂族金属的精炼技术包括铂族金属与贱金属的分离和铂族金属的相互分离。一般情况下,铂族金属以 络阴离子 的形态存在于溶液中,而贱金属以水合阳离子存在于溶液中,铂族金属与贱金属的化学性质差别很大,贵贱金属之间的分离相对简单,但铂族金属有相似的化学特性,因此铂族金属元素之间的相互分离很困难。常用的铂族金属精炼技术有:化学沉淀、结晶、溶剂萃取、离子交换、电化学沉积、分子识别、氧化蒸馏、高温熔炼等方法 ,例子如下: (2)一种合成方法,可以还原和稳定铂金纳米粒子,然后在β-D-葡萄糖水溶液中自组装成纳米线。水热处理启动了分散在pH8.0的β-D-葡萄糖溶液中的铂(IV)离子的还原。铂金纳米粒子被氧化的 葡萄糖 分子所稳定。铂金纳米粒子继续生长为纳米线,然后转变为具有粗糙针状表面的立方体纳米晶体。 (3)铂金纳米晶体可以在SC/超临界/ CO₂ 中直接通过被捕集沉淀来合成。 (4)通过同时加入封盖聚合物材料,可以实现从氯化铂中高效制备稳定的纳米铂粒子分散体。
(5)通过绿色配方合成了单分散的铂金纳米粒子(PtNPs)。使用葡萄糖作为还原剂,淀粉作为稳定剂,在缓冲水溶液中保护新形成的PtNP粒子。该合成反应简单、环境友好、重现性高、易于放大。这种铂金纳米粒子可以被转移到碳支持材料上,对碳的高比表面积要求不高。这使得利用石墨化碳黑来制备分散良好的Pt/C催化剂成为可能,这种催化剂在模拟燃料电池条件下的加速老化测试中表现出明显的耐久性。
铂合金 约在1779年,阿恰德熔化铂与磷、贡、砷等元素的混合物,制备得相应的低熔点铂合金,如采用 碳酸钾 作为助熔剂,熔化铂和砷的化合物,得到铂-13%(质量分数)砷(铂-28%( 摩尔分数 )砷)共晶合金,它的熔点仅为597°C。蒸发掉合金中的砷,他得到海绵铂并用于制备铂坩埚,这个过程持续到1810年。在铂的熔炼技术发展以后,人们便采用熔炼技术制造了更大的铂锭和更多的铂合金。1798年制造了千克铂质量标准原器;1862年制备成功铂-铱合金并发现铱对铂有重要的强化效应;1874年熔炼和铸造高纯铂-铱合金,铸锭尺寸达142cmx18cmx8cm,质量达236kg,用此合金铸锭制造了国际标准米原器和千克质量标准原器。 铂铱合金 的制备工艺流程包括:第一步选用纯度高的原材料;第二步,将所有原材料先进行高频真空熔炼后进行中频真空精炼,熔炼是铂铱合金制备的关键环节,对制作出来的铂铱合金的质量产生了重要的影响,因此要精心选择 。
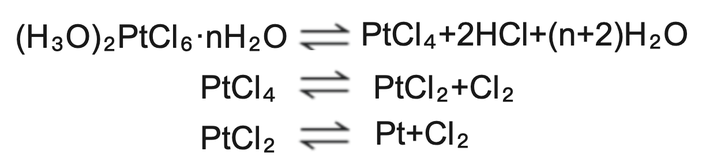
氯化物 氯铂酸经 铵盐 (如氯化铵)处理后,会产生 氯铂酸铵 。氯铂酸铵在氨溶液中的可溶性较低。在氢气中经加热后,氯铂酸铵会还原成铂金属。氯铂酸在被加热时,会经过 四氯化铂 和 二氯化铂 ,再分解成单质铂元素 :
氟化物 六氟化铂(PtF₆)是一种暗红色晶体,易挥发,是很强的氧化剂和 氟化剂 ,可以由金属铂与氟气制备 : 二溴化铂(PtBr₂)是一种深棕色或深绿色固体,结构为六方晶系/正交晶系,不溶于水和 酒精 ,可以由 溴铂酸 在280°C下分解而成。 四溴化铂(PtBr₄)是深红色至深紫色固体,结构为正交晶系,可以由溴铂酸(由铂和 氢溴酸 反应而成)和溴反应而成。
氧化物 氧化亚铂(PtO)可以通过加热二氧化铂至大约400℃制得:
氧化亚铂也可借由加热氢氧化亚铂制得:
二氧化铂(PtO₂)也称亚当斯催化剂或 氧化铂 ,通常以一水合物的形式存在,是有机合成中氢化和氢解反应的催化剂,深褐色粉末。由氯铂酸或氯铂酸铵和 硝酸钠 在500℃时共熔制备。首先生成 硝酸铂 ,后者再分解放出 氮氧化物 和氧气,得二氧化铂。产物呈棕色饼状,需水洗以除去 硝酸盐 。
硫化物 一硫化铂(PtS)或者二硫化铂(PtS₂)可以由硫和铂反应而成。
配合物 铂元素可以形成多种类型的配合物。如卤配合物、含氮和含氧的配合物、含磷的配合物,与CO形成 羰基化合物 、与不饱和的烯形成有机金属化合物等。这几种元素以生成氯配合物最为常见,将铂与碱金属的氯化物在氯气流中加热即可生成氯配合物。其中尤为重要的是H₂PtCl₆及其盐,棕红色的氯铂酸是Pt(IV)化学中最常用的起始物料。将海绵状金属铂溶于王水或氯化铂溶于盐酸都可生成氯铂酸: 在铂(IV)化合物中加碱可以制得 氢氧化铂 ,它具有两性,溶于盐酸得氯铂酸,溶于碱得到铂酸盐。 将NH⁺、K⁺、 Rb ⁺、Cs⁺等氯化物加到氯铂酸中生成难溶于水的黄色 氯铂酸盐 ,分析化学中常用H₂PtCl₆检验NH⁺、K⁺、Rb⁺、Cs⁺等离子;工业上还可常用加热分解氯铂酸铵来分离提纯金属铂。
应用领域
催化剂 催化剂是铂族金属最大用途,在石油化工中用于加氢、去氢化、异构化、环化、氧化、裂解、脱羧、脱氨基等反应中,生产各种特殊用途的石油化工产品。用 铂催化剂 重整几乎生产了全世界汽车和内燃机所需的全部高辛皖值汽油,含铂、铂钯、铂铑钯的催化剂可以净化汽车和柴油机排放的毒性尾气。
传感器 铂金属,半导体和导体聚合物形成的一维纳米结构,如纳米线和纳米棒,具有独特的电、光、磁和机械特性,在纳米器件中具有潜在的应用。由Pt参与制备的合金纳米自组装材料被广泛应用于化学、生物传感器等许多领域。由于铂在温度变化时自身电阻值也随之改变,铂也可以用作电阻 温度传感器 ,这种传感器很精确和稳定,它的线性度优于热偶和热敏电阻,可用来测量空气、土壤和水的温度。
电极材料 铂铑合金 是最重要的铂族金属材料,主要用于制备测温热电偶和编织催化网、铂铱、铂铑、铂钯合金有很高的抗电弧烧损能力,被用作电接点材料,铂铱合金和 铂钌合金 用于制造航空发动机 火花 钛阳极 代替 电解槽 中的 石墨阳极 可提高电流效率。
体内活性物质示踪剂 生物体内存在一些进行信号传递、代谢调控的活性分子,当这些活性物质超出限定范围,可能会导致产生疾病,甚至是癌症,因此针对体内这些活性物质的追踪和监测,对于疾病的发现和发病机制的研究具有重要意义。目前,在活性物质示踪领域,金属配合物发光探针因其灵敏度高、稳定性好等优点成为研究热点。Law团队设计了一种阴离子炔基铂(I)配合物作为生物探针,用于胰蛋白酶的检测。在2019年
药物 铂类抗癌药物,包括 卡铂 、顺铂和 奥沙利铂 ,可以用于治疗多种癌症,包括膀胱癌、 宫颈癌 、结直肠癌、头癌、肺癌、颈癌、卵巢癌和睾丸癌。 。它们在癌症治疗中非常有效;但是长期使用会产生耐药性。此外,还会遇到限制剂量的副作用,这些副作用包括顺铂的肾毒性和耳毒性、卡铂的骨髓抑制和奥沙利铂的神经毒性(周围神经系统的损伤) 。 此外,还可以观察到一些常见的副作用,如脱发、急性过敏反应、心脏毒性(心肌损伤)、血细胞减少、腹泻、肝毒性(肝损伤)、粘膜炎、恶心、疼痛、口腔炎和呕吐 。因此目前正处于从传统铂类抗癌药物到创新型抗癌药物的研究之中,比如开展反式铂和四价铂的抗癌药物研究,相信经过全世界科研人员的不懈努力,未来
其他应用 铂铑合金可用于生产 玻璃纤维 坩埚 和特种光学玻璃。铂金还被用在玻璃制造工业和玻璃纤维的生产,以及珠宝首饰中的戒指和宝石镶嵌。在牙科和医学领域,铂金被用于牙科和神经系统的修复,用于记录电活动,以及用于 心脏起搏器 电极。
安全事宜
毒性 铂对人类的毒理学影响仅限于其某些卤化物复合物和抗肿瘤剂顺铂及其类似物。卤化铂具有致敏作用。一位照相馆的工人在处理用复合铂盐处理过的纸张时,出现了鼻子和喉咙的刺激和呼吸困难。在四家英国炼油厂的研究中,91名接触复合铂盐的工人中有52人表现出反复打喷嚏、流鼻涕、胸闷、气喘呼和吸短促的症状,其中一部分人出现了带有 荨麻疹 的鳞状红斑皮炎症。随后的研究显示,在在职业性接触复杂的铂盐之后,也出现了眼睛流泪、打喷嚏、流鼻涕、咳嗽、喘息、呼吸困难和严重哮喘等症状。从最初接触铂到出现症状的潜伏期从几周到几年不等,症状会随着接触时间的增加而恶化。另外吸烟会增加接触铂金的工人的致敏风险。由于排放的铂金很可能是金属形式的,因此 汽车催化剂 排放的铂金的致敏潜力可能非常低。目前还没有关于从汽车 催化转化器 或工业排放的铂金可能在环境中转化为复合卤化物盐的信息。与卤化铂盐相比,用于癌症化疗的顺铂会引起肾脏毒性,包括肾小管和肾小球的病变,严重的恶心和呕吐,耳鸣和听力损失,以及感觉性周围神经病变。虽然卡铂的肾毒性较小,但它也会引起骨髓抑制。
监管措施 铂金的最高接触水平发生在通过吸入的职业接触工人身上,以及通过静脉注射铂金化疗药物治疗的病人身上。关于职业接触,铂盐的时间加权平均阈限值(TWA-TLV)是2 μg/m³金属铂是1 mg/m³。在英国,有人建议将金属铂作为可吸入粉尘总量的职业接触限值(8小时TWA)为5 mg/m³,将铂盐中的铂金限值为2 μg/m³。