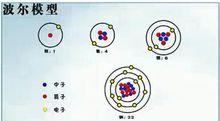
早期
20世纪早期,从做化学实验发现,对于原子或分子,假若电子数量是偶数,而不是奇数,则这原子或分子会更具化学稳定性(chemical stability)。1914年,约翰内斯·里德伯建议,主量子数为 4 的电子层最多只能容纳 32 个电子,但是他并不清楚为什么会出现因子。:197
1916年,吉尔伯特·路易斯在论文《原子与分子》(The atom and the Molecule)里表述出六条关于化学行为的假定,其中,第三条假定表明,“原子倾向于在每个电子层里维持偶数量的电子,更特别倾向于维持8个电子对称性地排列于立方体的8个顶点。”但是,他并没有试图预测这模型会造成什么样的光谱线,而任何模型的预测都必须符合实验结果。:198 化学家欧文·朗缪尔于1919年提议,将每个电子层按照其主量子数 分为 个同样体积的“细胞”,每个细胞都固定于原子的某个区域,除了最内部电子层的细胞只能容纳1个电子以外,其它每个细胞都可容纳2个电子。比较内部的电子层必须先填满,才可开始填入比较外部的电子层。 1913年,尼尔斯·玻尔提出关于氢原子结构的波尔模型,成功解释氢原子线谱,他又试图将这理论应用于其它种原子与分子,但获得很有限的结果。经过漫长九年的研究,1922年,玻尔才又完成关于周期表内各个元素怎样排列的论述,并且建立了递建原理,这原理给出在各个原子里电子的排布方法──每个新电子会占据最低能量空位。但是,波尔并没有解释为什么每个电子层只能容纳有限并且呈规律性数量的电子,为什么不能对每个电子都设定同样的量子数?:203 *589.6nm的谱线是2P1/2态向2S1/2态跃迁产生的谱线。
*589.0nm的谱线是2P3/2态向2S1/2态跃迁产生的谱线。
由于弱外磁场作用,2S1/2态能级会分裂成两个子能级,2P1/2态也会分裂成两个子能级,但由于两个态的朗德g因子不同,因此会形成4条不同谱线。由于外磁场作用,2P3/2态能级会分裂成四个子能级,但是从2P3/2的+3/2态不能跃迁至2S1/2的-1/2态,从2P3/2的-3/2态不能跃迁至2S1/2的+1/2态,因此总共会形成6条不同谱线。